Experten des öffentlichen Gesundheitswesens sind besorgt über die übereilte FDA-Zulassung des Impfstoffs
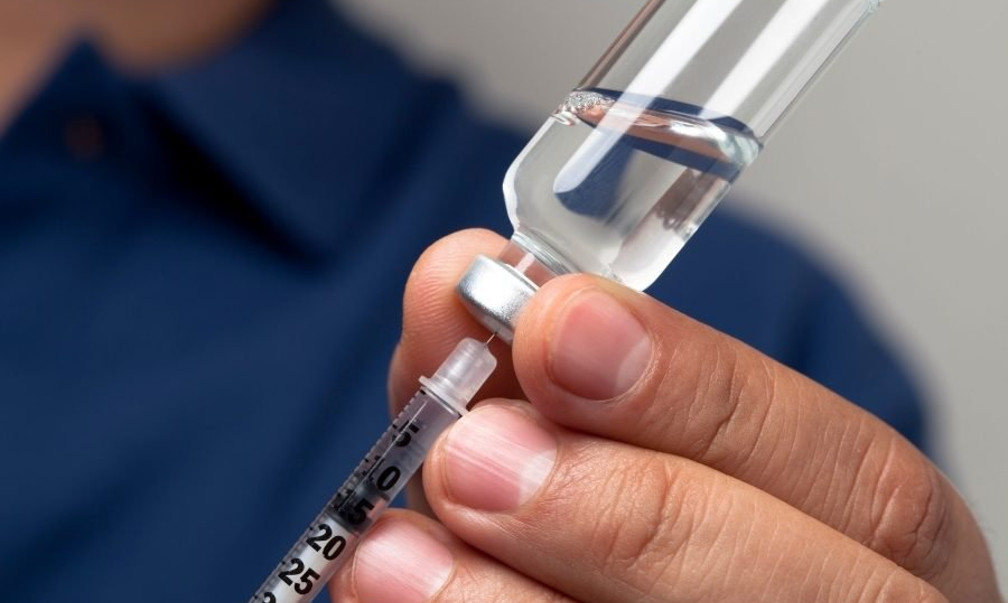
Der Impfstoffversuch, den Vizepräsident Mike Pence am Montag in Miami begonnen hat, gibt den Vereinigten Staaten eine winzige Chance, sich darauf vorzubereiten, Millionen von Amerikanern kurz vor dem Wahltag zu impfen.
Diese Möglichkeit entsetzt viele Gesundheitsexperten.
Zu ihren Bedenken gehören: Frühe Beweise dafür, dass ein Impfstoff wirkt, werden zu politischem Druck der Verwaltung führen, um eine Notfallfreigabe durch die Food and Drug Administration zu erhalten. Dieser Konflikt zwischen Wissenschaft und Politik könnte dazu führen, dass einige Menschen dem Impfstoff misstrauen und ihn ablehnen, wodurch die globale Kampagne zu seiner Beendigung untergraben wird. Oder es kann zu einem Produkt führen, das nicht vollständig schützt. Das bereits erschütterte Vertrauen in routinemäßige Kinderimpfungen könnte weiter sinken.
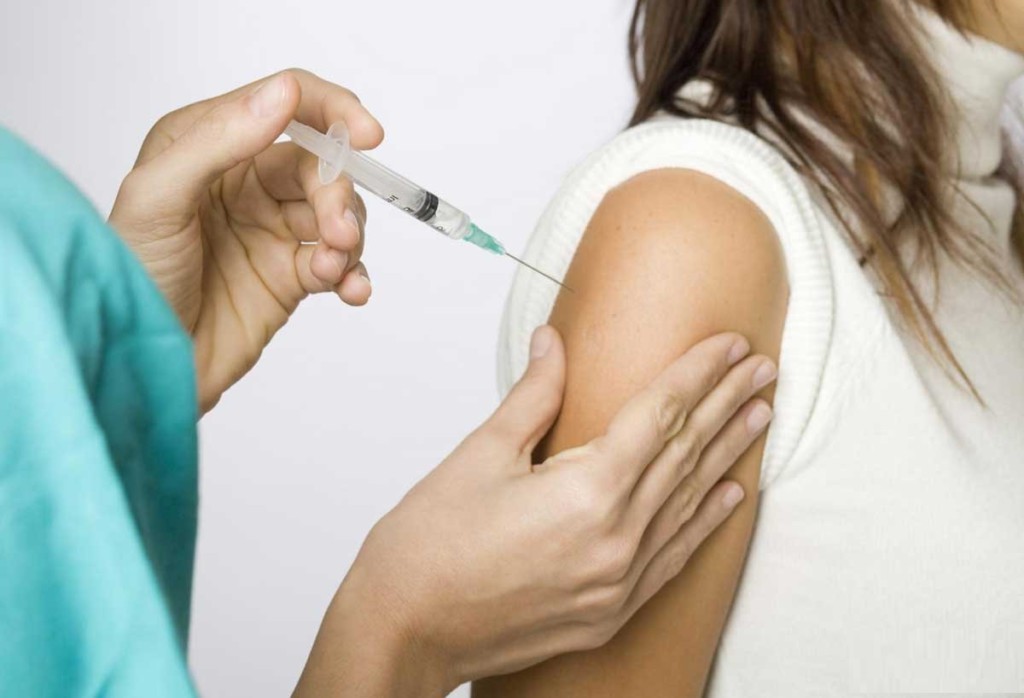
„Die Befürchtung ist, dass Sie mit dem Impfstoff das tun werden, was [Trump] bereits mit der [Eröffnung] der Schule getan hat“, sagte Dr. Joshua Scharfstein, ein ehemaliger stellvertretender FDA-Kommissar und Professor an der Johns Hopkins University in Baltimore. „Nimm ein wichtiges, schwieriges Thema und politisiere es. Das will man vermeiden.“
Am Montag um 6:45 Uhr wurde der erste Freiwillige der Phase 3 der historischen Impfstoffstudie von Moderna Therapeutics in einer Klinik in Savannah, Georgia, geimpft. Ärzte in 88 anderen medizinischen Einrichtungen, von Miami bis Seattle, bereiteten sich ebenfalls darauf vor, einen experimentellen Impfstoff in einer Studie mit 30.000 Personen bereitzustellen.
Arzt. Anthony Fauci, der führende Experte des Landes für Infektionskrankheiten, sagte Reportern, er hoffe, dass bis Ende der Woche 15.000 Menschen geimpft würden, obwohl er keine Informationen über Fortschritte bei der Erreichung dieses Ziels lieferte. Alle Freiwilligen erhalten 29 Tage nach der ersten Impfung eine zweite Impfung. (Die Hälfte erhält ein Placebo mit Kochsalzlösung.)
Ein weiterer Impfstoff, der von Pfizer in Zusammenarbeit mit dem deutschen Unternehmen BioNTech hergestellt wird, trat diese Woche ebenfalls in eine große Phase-3-Studie in den USA ein. Es wird unabhängig von den National Institutes of Health getestet, die die Moderna-Impfstoffstudie teilweise finanzieren, sowie die Oxford University/AstraZeneca-Impfstoffstudie und andere zukünftige Studien. AstraZeneca sagte, einige Dosen seines Impfstoffs könnten bereits im September fertig sein.

Fauci sagte, er erwarte, dass die Moderna-Studie bis Ende des Jahres eine Antwort darauf geben werde, ob der Impfstoff wirken werde – und könne wahrscheinlich im Oktober eine Antwort erhalten. „Ich bezweifle es, aber wir sind nicht sicher, ob es möglich ist.“
Diese Schnelllebigkeit beunruhigt einige Experten.
„Ich sehe nicht, wie dies auch nur annähernd möglich ist, es sei denn, was ich am meisten befürchte, das ist eine verkürzte Phase-3-Studie mit nur einer Darstellung der Wirksamkeit, mit einer Darstellung häufiger Nebenwirkungen, und dann wird sie eingeführt. “, sagte Arzt. Paul Offit, Direktor des Vaccine Education Center, Children’s Hospital of Philadelphia.
Pence spielte diese Bedenken am Montag herunter und sagte Reportern: „Es wird keine Kürzungen geben. Es wird keine Abstriche geben.“
Die Beamten bestehen auf einem offenen und transparenten Verfahren.
Rep. Raja Krishnamurthy (R-Ill.), Vorsitzender des House Oversight and Reform Subcommittee on Economic and Consumer Policy, bereitet die Veröffentlichung von Gesetzen vor, die die FDA dazu verpflichten, jeden COVID-Impfstoff von einem Expertengremium prüfen und eine Empfehlung vor dem FDA-Kommissar abgeben zu lassen Stefan Hahn. trifft eine Entscheidung.
Bei früheren Impfstoffen hat sich die FDA in der Regel auf ein solches Komitee verlassen, das sich hauptsächlich aus Impfstoffexperten zusammensetzt und vom FDA-Beauftragten ernannt wird. Sie prüfen normalerweise alle Beweise gründlich, bevor sie darüber abstimmen, ob die FDA einen Impfstoff genehmigen soll. Der Kommissar ging selten, wenn überhaupt, gegen die Entscheidungen des Komitees vor.
Khan untergrub Anfang des Jahres das Vertrauen in die Unabhängigkeit der FDA, glaubten viele Beobachter, als er eine Notfallzulassung für Hydroxychloroquin herausgab, ein Medikament zur Behandlung von Malaria, das Präsident Donald Trump und Mitglieder seiner Regierung weiterhin förderten. fälschlicherweise als Heilmittel für COVID-19. Später entzog die FDA die Zulassung, die ohne Rücksprache mit einem unabhängigen Gremium erfolgte.
„Die Unabhängigkeit der FDA ist eindeutig durch die Hydroxychloroquin-Problematik bedroht“, sagte Dr. Jesse Goodman, Professor an der Georgetown University, der die Biologicals Division der FDA leitete und später Chief Scientist war.
Die Agentur sollte externen Wissenschaftlern und der Öffentlichkeit die Möglichkeit geben, die Daten und Argumente der FDA zu überprüfen, bevor sie eine solche Entscheidung trifft, sagte er.
Bedenken hinsichtlich politischer Einmischung tauchten kürzlich auf, als Trump aufgeregt über einen Impfstoff sprach und Finanzminister Steven Mnuchin Reportern zuversichtlich sagte, dass es bis Ende des Jahres einen Notfallimpfstoff geben werde.
Natürlich wird die FDA wahrscheinlich nicht versucht sein, eine Notfallfreigabe zu erteilen, ohne dass Daten zeigen, dass der Impfstoff wirkt und keine schwerwiegenden Nebenwirkungen verursacht.
Massive Ausbrüche in Texas und anderen stark betroffenen Gebieten, in denen der Impfstoff von Moderna getestet wird, sollten eine Antwort geben, obwohl wann genau eine offene Frage ist.
Theoretisch könnten Wissenschaftler die Wirksamkeit eines Impfstoffs verstehen, bevor alle 30.000 Menschen registriert, geimpft und untersucht worden sind.
Tatsächlich könnte die Antwort klar werden, sobald es nur noch 150 bis 160 Fälle unter den Studienteilnehmern gibt, sagte Fauci. Wenn etwa zwei Drittel dieser Fälle bei nicht geimpften Personen auftreten würden, würde dies den Statistikern zeigen, dass der Impfstoff zu mehr als 60 % wirksam war.
Wenn ein Impfstoff zu 80 % bis 90 % wirksam ist und die jährliche Infektionsrate an den Orten, an denen er getestet wird, mehr als 4 % beträgt, könnten Wissenschaftler eine Wirksamkeit in einer solchen Studie signalisieren, die nur 50 Fälle oder „nur drei Monate“ umfasst – sagte Ira Longhini, ein Biostatistiker an der Universität von Florida, der Impfstoffversuche entwickelt.
Die Impfstoffversuche von Moderna werden diese Dreimonatsschwelle am 27. Oktober erreichen.
Das Schicksal der Studie liegt zum Teil in den Händen ihres 30-köpfigen Data and Safety Monitoring Board, dessen Mitglieder nicht-blinde Daten über Teilnehmer in Echtzeit einsehen können – zum Beispiel feststellen, wer mit einem echten Impfstoff geimpft wurde und stürzt krank. Das Gremium wird das NIH und den Impfstoffhersteller benachrichtigen, wenn es unerwartete Daten sieht, entweder gefährliche Nebenwirkungen oder hohe Wirksamkeit. Einige befürchten, dass die FDA unter Druck gesetzt wird, die Studie zu stoppen, wenn sich der Impfstoff in den frühen Testphasen als wirksam erweist.
Offit sagte, die NIH sollten nichts anderes als einen abgeschlossenen Prozess mit 30.000 Menschen akzeptieren. Fünfzig Fälle seien eine „sehr kleine Zahl“, die als Beweis für die Freigabe eines Impfstoffs verwendet werden könne, der zig Millionen Menschen verabreicht werden könnte, sagte er.
Die Öffentlichkeit konnte die Freigabe jedes wirksam erscheinenden Impfstoffs verlangen. Moderna sagte, es habe bereits mit der Produktion von Millionen Dosen des Risikoimpfstoffs begonnen und auf den Erfolg des Impfstoffs gesetzt. Die FDA könnte diejenigen freilassen, denen die Befugnisse erteilt wurden, als das Land im März einen öffentlichen Gesundheitsnotstand ausrief.

Da mehr als die Hälfte des Landes Trump gegenüber zutiefst misstrauisch ist, zeigen jüngste Umfragen, dass jede Bundesentscheidung auf Widerstand stoßen und zu einer weit verbreiteten Ablehnung selbst eines vielversprechenden Impfstoffs führen könnte. Scharfstein macht sich Sorgen über die „reflexartige“ Reaktion der Demokraten auf den Impfstoff, wenn Trump vor der Wahl dafür wirbt.
Experten sind auch besorgt über die Freigabe eines Impfstoffs, der einige positive Wirkungen zeigt, aber keinen zuverlässigen Schutz bietet. Eine Folie, die Anfang dieses Monats vom stellvertretenden FDA-Direktor Philip Krause von der Weltgesundheitsorganisation vorgestellt wurde, besagte, dass ein schwacher Impfstoff die Öffentlichkeit möglicherweise nicht richtig schützt, was zu einem falschen Sicherheitsgefühl für diejenigen führt, die ihn erhalten, und es schwieriger macht, ihn zu testen. zukünftige Impfstoffe.



0 Kommentare